İlaca Duyarlı CAR T Hücreleri: Daha Güvenli ve Kontrollü İmmünoterapi İçin Yeni Bir Yaklaşım
Kimerik antijen reseptörü (CAR) T hücreleri, özellikle hematolojik malignitelerde devrim niteliğinde sonuçlar ortaya koymuş hücresel immünoterapi yaklaşımlarıdır. Bununla birlikte, solid tümörlerde sınırlı etkinlik göstermeleri, sağlıklı dokulara yönelik istenmeyen sitotoksisite (on-target/off-tumor toksisite) ve sitokin salınım sendromu (CRS) gibi ciddi yan etkiler, bu tedavi yönteminin klinik kullanımını kısıtlayan temel sorunlar arasında yer almaktadır.
Bu zorlukları aşmaya yönelik olarak, École Polytechnique Fédérale de Lausanne (EPFL) bünyesinde, Melita Irving ve Greta Maria Paola Giordano Attianese liderliğinde geliştirilen yeni bir teknoloji, CAR T hücre aktivitesinin klinikte hâlihazırda kullanılan bir ilaç aracılığıyla geri dönüşümlü olarak kontrol edilmesini mümkün kılmaktadır. “DROP-CAR” (Drug-Regulated Off-switch Protein–Protein Interaction CAR) olarak adlandırılan bu sistem, bulgularıyla Nature Chemical Biology dergisinde yayımlanmıştır.
DROP-CAR Teknolojisinin Temel Prensibi
Klasik ikinci nesil (2G) CAR tasarımlarında, antijen tanıyan tek zincirli değişken fragman (scFv), hücre içi CD3-ζ ve ko-stimülatuvar domainler (örneğin CD28) ile birleştirilerek sürekli aktif bir sitotoksik yanıt oluşturur. Ancak kronik antijen maruziyeti T hücre tükenmesine (exhaustion) yol açabilmekte ve yüksek antijen yoğunluğunda aşırı immün yanıt gelişebilmektedir.
DROP-CAR sisteminde ise kontrol mekanizması hücre dışı protein–protein etkileşimi (PPI) üzerinden sağlanmaktadır. Bu tasarımda:
- CAR’ın hücre dışı kısmında yer alan dmLD3 adlı insan kökenli tasarlanmış bir protein domaini,
- Yüksek afinite ile BCL-2 proteinine bağlanmaktadır.
- Klinik kullanımda olan Venetoclax ise bu dmLD3–BCL-2 etkileşimini bozarak CAR yapısının ayrışmasına neden olur.
Sonuç olarak:
- Venetoklaks uygulandığında → CAR yapısı parçalanır ve T hücresi aktivitesi baskılanır.
- İlaç kesildiğinde → CAR yeniden assemble olur ve T hücreleri antitümör aktivitesini geri kazanır.
Bu mekanizma, hücreyi öldürmeden veya sinyal iletim zincirini degradasyona uğratmadan, doğrudan tümör hücresi ile temas düzeyinde kontrol sağlamaktadır.
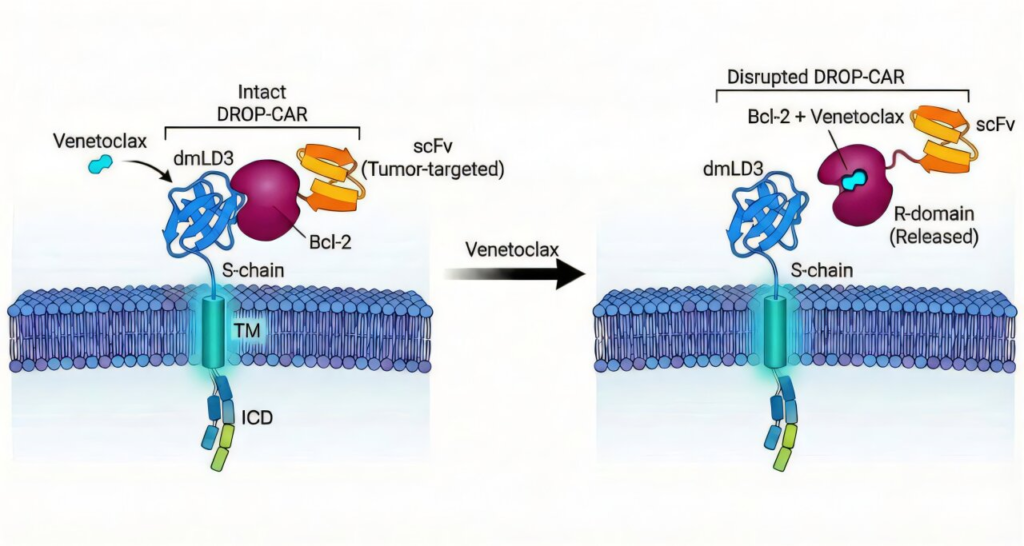
Şekil 1: DROP-CAR (Drug-Regulated Off-switch Protein–Protein Interaction CAR) sisteminin şematik gösterimi. CAR’ın hücre içi sinyal iletim bileşeni, bir transmembran (TM) domain aracılığıyla hücre yüzeyinde bulunan sinyal zincirine (S-chain) bağlanmıştır. S-chain’in uç kısmında, hesaplamalı protein tasarımı ile geliştirilmiş insan kökenli bir protein domaini olan dmLD3 yer almaktadır. dmLD3, yüksek afinite ile BCL-2 proteinine bağlanmaktadır. CAR’ın antijen tanıyan reseptör domaini (R-domain) ise dmLD3 tarafından tanınan BCL-2 motifini içermektedir. Bu spontan protein–protein etkileşimi sayesinde CAR yapısı bütünlüğünü korur ve antijen bağlanması durumunda T hücresi aktivasyonu gerçekleşir. Klinikte kullanılan bir BCL-2 inhibitörü olan venetoklaks uygulandığında, dmLD3–BCL-2 etkileşimi kompetitif olarak bozulur. Bunun sonucunda CAR kompleksi ayrışır, hücre–hücre teması kesintiye uğrar ve CAR T hücresinin sitotoksik aktivitesi geçici olarak baskılanır. Venetoklaksın ortamdan uzaklaştırılmasıyla birlikte protein–protein etkileşimi yeniden kurulur, CAR yapısı tekrar assemble olur ve antitümör aktivite geri kazanılır. Bu tasarım, CAR T hücrelerini ortadan kaldırmadan, hücre yüzeyi düzeyinde uzaktan, geri dönüşümlü ve farmakolojik olarak kontrol edilebilir bir güvenlik mekanizması sunmaktadır. (Kaynak: Ludwig Cancer Research)
Preklinik Bulgular
DROP-CAR T hücreleri hem in vitro sistemlerde hem de murin tümör modellerinde test edilmiştir. Çalışma sonuçları şunları göstermiştir:
- Venetoklaks uygulaması ile CAR T hücre aktivitesi etkin şekilde baskılanabilmektedir.
- İlaç kesildikten sonra antitümör etkinlik geri kazanılmaktadır.
- İleri evre tümör modelinde dahi tümör kontrolü yeniden sağlanabilmiştir.
- Baskılama etkisi geri dönüşümlüdür (reversible).
Klinik ve Biyolojik Önemi
Bu sistemin potansiyel avantajları şunlardır:
- On-target/off-tumor toksisitenin azaltılması
- Sitokin salınım sendromu riskinin kontrol altına alınması
- T hücre tükenmesinin önlenmesi amacıyla “dinlenme aralıkları” sağlanabilmesi
- İnsan kökenli protein bileşenleri kullanılması sayesinde immünojenisite riskinin azaltılması
- Klinik olarak onaylı bir ilacın kullanılması nedeniyle translasyonel potansiyelin yüksek olması
DROP-CAR teknolojisi, hücresel immünoterapilerde çoklu girişli (multi-input) kontrol sistemlerinin geliştirilmesine olanak tanıyan modüler bir platform sunmaktadır.
Sonuç
İlaca duyarlı ve geri dönüşümlü olarak kontrol edilebilen DROP-CAR sistemi, CAR T hücre tedavisinin güvenlik profilini iyileştirmeye yönelik yenilikçi bir yaklaşım sunmaktadır. Solid tümörler dahil olmak üzere daha geniş hasta gruplarında kontrollü ve güvenli uygulamaların önünü açabilecek bu teknoloji, immünoterapi alanında önemli bir translasyonel adım olarak değerlendirilmektedir.
Makale: Drug-controlled CAR T cells through the regulation of cell–cell interactions
Kaynak:https://www.genengnews.com/news/drug-controlled-car-t-cells-may-enable-safer-immunotherapy/